Científicos norteamericanos combinaron la cepa Wuhan con Ómicron para saber por qué genera cuadros más leves
Investigadores de la Universidad de Boston crearon un virus híbrido con el objetivo de determinar en qué partes del patógeno residen las particularidades que lo hacen más transmisible, pero menos grave. El estudio fue realizado en ratones y difundido en un preprint
Según indicaron en el trabajo que se desarrolló en ratones y que fue publicado en bioRxiv como preprint, que aún no cuenta con validación de pares, este “nuevo” patógeno “se replica de manera eficiente en líneas celulares y células pulmonares”, siendo que “las mutaciones en (la proteína) S no explican completamente la capacidad de replicación atenuada de Ómicron en células humanas cultivadas”.
“La variante Ómicron (BA.1) del SARS-CoV-2, predominante a nivel mundial y recientemente identificada, es altamente transmisible, incluso en personas completamente vacunadas, y causa una enfermedad atenuada en comparación con otras variantes virales importantes reconocidas hasta la fecha”, afirmaron los científicos en el documento, al tiempo que indicaron que el objetivo de esta investigación era determinar si “el escape de la vacuna de Ómicron se define por mutaciones en S” o si “los principales determinantes de la patogenicidad viral residen fuera de S”.
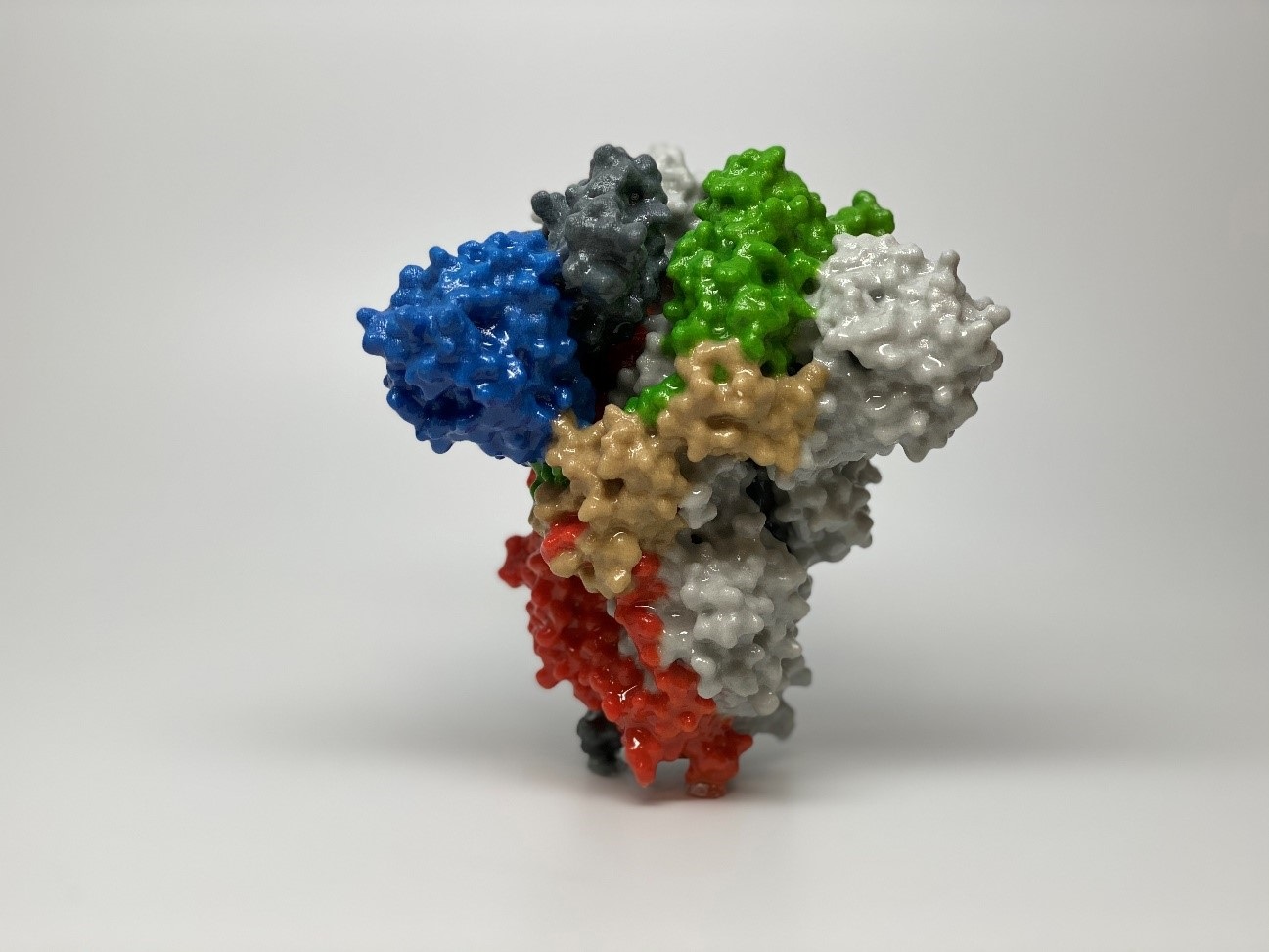
Los científicos explicaron que la proteína espiga (S) de Ómicron cuenta con “un número inusualmente grande de mutaciones”, las cuales son consideradas como “principales impulsores de estos fenotipos”. Es por eso que, para determinar su comportamiento, los investigadores de Boston generaron un “SARS-CoV-2 recombinante quimérico que codifica el gen S de Ómicron en la columna vertebral de un aislado ancestral de SARS-CoV-2″. O dicho en otras palabras, combinaron a la versión BA.1 de Ómicron con el virus surgido en Wuhan.
Los resultados fueron determinantes, “el virus portador de Ómicron S escapa con fuerza a la inmunidad humoral inducida por la vacuna”, es decir que evade la respuesta inmune que genera la vacunación, como consecuencia de las mutaciones que presenta en “la unión al receptor (RBM)”. Esto último ocurre como consecuencia de las particularidades que tiene en la corona (que le da nombre al patógeno).
Hasta aquí, según indicaron, su comportamiento fue igual a la BA.1 original. Sin embargo, la denominada Ómicron S demostró que “se replica de manera eficiente en líneas celulares y células pulmonares distales de tipo primario”, es decir que esta combinación “inflige una enfermedad grave con una tasa de mortalidad del 80%”. “Esto indica que, si bien el escape de la vacuna de Ómicron se define por mutaciones en S, los principales determinantes de la patogenicidad viral residen fuera de S”, explicaron. Dicho de otra manera, mientras que la capacidad de infectar se encuentra en la proteína S, su letalidad no está en ese lugar.
Paso a paso: qué buscaron los científicos
Las razones de su investigación quedaron claras. Sin embargo, para determinar los resultados desarrollaron una serie de pasos. Luego de dar cada uno, realizaron un análisis y brindaron conclusiones.
El primer escalón que dieron los científicos fue comparar “la eficiencia de infección de Omi-S con un virus ancestral y Ómicron en cultivo celular”, para esto utilizaron microscopios y células infectadas con estos patógenos. “El virus ancestral [en lo sucesivo, de tipo salvaje (WT)] y Omi-S se propagaron rápidamente en las células”, señalaron los científicos y advirtieron que, tras 24 horas, el primero produjo una infección del 89% de las células, mientras que el otro evidenció un 80 %. En tanto, Ómicron “se replicó más lentamente, lo que provocó un 48 % de células infectadas”.
“El ensayo de placas mostró que aunque tanto Omi-S como Ómicron produjeron niveles más bajos de partículas virales infecciosas en comparación con virus ancestral, el título viral de Omi-S fue significativamente mayor que el de Ómicron”, explicaron los investigadores. “Estos resultados indican que, si bien las mutaciones en la proteína S influyen en la eficacia de infección de Ómicron, no explican por completo el comportamiento de infección de Ómicron en cultivo celular”, concluyeron tras este primer análisis.
El segundo paso fue ampliar el estudio a las células epiteliales de pulmón, “un importante sitio de replicación viral en pacientes con COVID-19 grave”, señalaron. Para analizar el comportamiento de los virus, los científicos utilizaron “células epiteliales alveolares de pulmón”, el cual es “esencial en el pulmón distal y constituye uno de los principales objetivos de la infección por SARS-CoV-2″. Los resultados corroboraron “la conclusión de que las mutaciones en S no explican completamente la capacidad de replicación atenuada de Ómicron en células humanas cultivadas”.
De todos modos, señalaron que, pese a que la literatura publicada advierte que “la inoculación intranasal de ratones (de 12 a 20 semanas de edad) con Ómicron no provoca una pérdida de peso significativa, la inoculación con el virus ancestral desencadenó una rápida disminución del peso corporal, perdiendo todos los animales más del 20% de su peso corporal inicial, a los 8 días después de la infección”.
Esta situación se evidenció en la versión “quimérica”. “Es importante destacar que el 80 % de los animales infectados con Omi-S también perdieron más del 20 % de su peso corporal a los 9 días”, señalaron. Al tiempo que resaltaron que la salud de los ratones infectados con el virus ancestral y Omi-S se vio deteriorada “rápidamente”. “De acuerdo con los resultados de la pérdida de peso corporal y la puntuación clínica, el virus ancestral y Omi-S causaron tasas de mortalidad del 100 % (6/6) y del 80 % (8/10), respectivamente” mientras que “todos los animales infectados con Ómicron sobrevivieron”. En consecuencia, según explicaron los científicos, “estos hallazgos indican que la proteína S no es el principal determinante de la patogenicidad de Ómicron en ratones”
Vale destacar que, según indicaron tras la investigación in vitro, “el título de virus infeccioso en los pulmones de ratones infectados con el virus ancestral fue mayor que el detectado en ratones infectados con otros dos virus. Notablemente, sin embargo, los ratones infectados con Omi-S produjeron 30 veces más partículas de virus infecciosos en comparación con ratones infectados con Ómicron”, aunque detectaron que esta variante, pese a producir una infección leve, puede ser “persistente”.
Otro punto relevante del estudio indica dónde se detectó la mayor cantidad de virus. “Mientras que el virus Omi-S causó una infección bronquiolar grave con alrededor del 15-20 % de los bronquiolos positivos para la proteína S en todos los ratones examinados, menos del 1 % de los bronquiolos fueron positivos para S en ratones infectados con Ómicron”, señalaron los científicos. Al tiempo que indicaron que esta infección bronquiolar se asoció con necrosis epitelial (muerte de tejido corporal) para los roedores infectados con Omi-S, una situación que no se evidenció en la versión BA.1.
“Esto sugiere que la replicación de Ómicron en los pulmones de los ratones, particularmente en los bronquiolos, está sustancialmente atenuada en comparación con Omi-S, lo que respalda nuestra conclusión de que las mutaciones en la proteína S son solo parcialmente responsables de la patogenicidad atenuada de Ómicron”, concluyeron los expertos. Al tiempo que advirtieron que “este estudio proporciona información importante sobre la patogenicidad” de la variante más reciente del SARS-CoV-2.
“En los ensayos de infección in vitro, el SARS-CoV-2 (Omi-S) ancestral portador de picos de Ómicron exhibe una eficiencia de replicación mucho mayor en comparación con Ómicron. De manera similar, en ratones, Omi-S contrasta con Ómicron no mortal y causa una enfermedad grave que provoca una mortalidad de alrededor del 80 %. Esto sugiere que las mutaciones fuera del pico son los principales determinantes de la patogenicidad atenuada de Ómicron en ratones”, concluyeron los científicos.


